2022年再生医学领域发展态势
- 来源:中国知网
- 阅读量:1004
- 发表时间:2023-03-22
再生医学领域经过多年的发展,在多种疾病治疗中展现出巨大应用潜力。近年来,大数据、学科融合等研究理念的不断渗透,以及一系列通用技术在再生医学领域的广泛应用,推动再生医学研究广度和深度持续拓展,领域范畴也不断拓宽,为该领域带来了全新的发展机遇。本文从科技规划、监管政策、科技及产业进展等角度,对再生医学热点领域 2022 年的发展趋势进行了分析,并对相关领域未来的发展进行了展望。
再生医学是一门交叉学科,旨在利用生命科学、 材料科学、工程学、计算机科学等多学科的理论和 方法,通过激活机体内源性干细胞,或植入外源干 细胞、干细胞衍生细胞、功能性组织器官,来修复、 替代和增强人体内受损、病变或有缺陷的组织和器 官,实现疾病治疗 。再生医学经过多年的发展, 已经展现出在多种疾病治疗中的巨大应用潜力。近 年来,大数据、学科融合等研究理念的不断渗透, 以及生命组学、基因编辑、高分辨率成像、新材料 制造等技术在再生医学领域的广泛应用,推动再生 医学研究的广度和深度持续拓展,领域范畴也不断 拓宽,为再生医学领域带来了全新的发展机遇,并 孕育更多生物产业增长点。
干细胞一直是近年来再生医学的核心方向,在经历了多年的密集布局和研究之后,该领域已经进 入平稳发展期,干细胞疗法的临床转化和产业化 发展正成为现阶段的重点。基于干细胞的类器官 (organoid) 和器官芯片 (organ-on-a-chip) 是在学科融 合不断深化的基础上发展起来的全新领域,其在生 物医药科研、临床治疗和药物研发等各个环节所展 现的应用潜力,在国际上迅速引发研究热潮,至今 已经发展至产业阶段,孕育巨大的产业价值。异种 器官移植是再生医学的传统领域,在发展停滞了 20 年之后,近年来开始焕发全新生机。本文将以再生 医学这三个前沿发展方向为核心,对 2022 年再生 医学领域的发展态势进行分析。
1 再生医学领域国际规划与监管现状
1.1 加快再生医学转化是各国生命科学战略部署的核心发展方向
再生医学领域是各国 / 地区生命科学战略布局 的核心组成部分,相关疗法开发和医学应用是当前 的重点布局方向。美国《国家生物技术和生物制造 计划》提出了推进再生医学等相关生物制品市场转化的行动目标。欧盟“地平线欧洲”(Horizon Europe) 计划健康领域 2021—2022 年工作计划支持开展评价多能干细胞治疗等先进疗法有效性、 安全性、作用方式的临床研究,2023—2024 年工作计划 则重点布局了以类器官、微生理系统 (microphysiological systems, MPS) 等技术为核心的 非动物技术的开发及其在生物医学研究中的应用。 日本内阁发布的《2022 年综合创新战略》在健康与医药战略性应用领域,重点支持再生医学领域 技术的临床应用推广,还强调了开发具有高分化效率或低免疫原性特征的下一代诱导多能干细胞 (induced pluripotent stem cells, iPSCs)、可用于个性化药物疗效评估的类器官等革命性新技术的重要性。韩国科学和信息通信技术部 (MSIT) 发布的《数 字生物创新战略》将干细胞治疗技术和类器官技术确定为12 大核心技术之一 ;韩国生命工学研究 院 (KRIBB) 同样将器官替代治疗技术 ( 类器官、异 种器官移植 ) 视为引领生物未来发展的技术 。澳 大利亚医疗研究未来基金 (MRFF) 2022—2031 年研 究计划重点支持开展干细胞转化研究,开发安全、有效的干细胞创新疗法 ;澳大利亚技术科学与工程院 (ATSE) 则建议将器官芯片技术列入澳大利亚 2022 年关键技术清单进行重点支持 。我国生物医药领域“十四五”规划中也多次提及发展干细胞与再生医学前沿技术,其中《“十四五”生物经济发 展规划》中明确提出支持发展干细胞治疗等新技术, 推动形成再生医学治疗新模式,《“十四五”医药工 业发展规划》中则重点支持发展干细胞治疗等生 物药的研发。
1.2 类器官模型应用前景广阔,相关研究获得各国科技研究经费的大力支持
类器官模型构建和基于类器官模型的药物评价 平台建设获得进一步资金支持。韩国生命工学研究 院计划在 2022—2025 年投入 40 亿韩元推动开发基 于类器官的毒性评估平台建设 。英国生物技术和 生物科学研究理事会 (BBSRC) 和动物实验替代、减少和优化国家中心 (NC3Rs) 投资 470 万英镑支持 下一代非动物技术开发,其中包括基于人类干细胞 的类器官系统和血管化器官芯片模型 。2022 年, 我国国家重点研发计划“干细胞研究与器官修复” 重点专项也对组织类器官高通量培养及应用、基于 干细胞的智能多器官芯片系统、基于干细胞的器官 互作模型、基于干细胞的肿瘤微环境类器官模型与 应用等方向进行了资助。
1.3 再生医学领域配套监管规范陆续出台,利好行业创新和规范化发展
随着技术的发展,干细胞领域的临床应用转化 正在稳步推进,类器官技术也逐步发展成为药物研 发中替代动物实验的关键工具 ;2022 年,相关配套 监管规范陆续出台,利好行业创新和规范化发展。 在干细胞技术领域,2022 年 9 月,第三届中国干细 胞与再生医学协同创新平台大会发布了干细胞领域 一系列相关标准,包括我国牵头制定的首个干细胞 国际标准 ISO 24603,以及 1 项国家标准和 7 项团体标准,对干细胞研究伦理以及干细胞及其衍生物 的关键质量属性和质量控制等进行了系统规范。 2022 年 10 月,我国国家药品监督管理局 (NMPA) 食品药品审核查验中心正式发布《细胞治疗产品生 产质量管理指南 ( 试行 )》,从产品生产的全过程明 确了包括干细胞在内的细胞治疗产品的生产质量管 理规范,进一步推进了我国细胞治疗产业的规范化 和加速发展。在类器官技术领域,美国众议院于 2022 年 6 月通过《2022 年食品和药品修正案》, 在药物研发相关条款中,将“动物实验”修改为“非 临床检测”,并在这一新概念中明确纳入了“器官 芯片和其他微生理系统”,这标志着器官芯片已经 成为美国食品药品监督管理局 (FDA) 认可的临床前 研究手段,动物实验不再是唯一的标准。在 2021 年底我国国家药品监督管理局药品审评中心 (CDE) 也首次将类器官列入相关产品的非临床技术指导原 则中,而我国首个关于类器官药物敏感性检测指导 肿瘤精准治疗临床应用的专家共识也于 2022 年 7 月面世,旨在进一步规范和推动类器官的临床应用与实践。
2 再生医学领域科技与产业发展现状
2.1 干细胞基础研究持续深入,产业进程不断加快
干细胞自我更新和分化的特性使其展现出治疗 多种疾病的潜能,也因此获得全球的关注。干细胞 领域正处于基础研究和临床转化同步发展的阶段, 干细胞治疗产业的上中下游布局日趋成熟,发展速度不断加快。2022 年,干细胞基础研究继续稳步推 进,对干细胞的认识日趋深入 ;同时,干细胞应用 基础研究广泛开展,干细胞在多种疾病中的治疗效 果获得进一步验证 ;在此基础上,干细胞临床研究 规模不断扩大,陆续有新药获得上市许可,干细胞产业愈发展现可观发展前景。
2.1.1 干细胞基础研究稳步推进
在干细胞基础研究方面,对于干细胞干性、分化等调控机制的探索进一步深化。其中,干细胞的定向分化调控一直是干细胞研究的重点。2022 年,科研人员进一步鉴定发现了多个调控干细胞定向分 化的关键分子机制,揭示了一系列调控胰腺谱系 和血液谱系分化的关键因子,同时还发现了促 进人胚胎干细胞(embryonic stem cells, ESCs) 定向 分化的调控通路。在此基础上,科研人员实现了 干细胞向多种细胞类型的定向分化,如实现了将大 鼠的多能干细胞 (pluripotent stem cells, PSCs) 分化成为原始生殖细胞样细胞 (primordial germ cell-like cells, PGCLCs),进而产生了功能性精子,并繁殖出 有活力的后代 ;将人 ESCs 和 iPSCs 诱导分化为处 于静息状态的肝星状细胞 (induced hepatic stellate cells, iHSCs),为体外肝纤维化模型构建奠定基础 。 此外,重编程领域在 2022 年也取得了一系列 突破。一方面,在体外人工构建出 iPSCs 之后,如何建立代表生命起点的全能干细胞成为进一步的攻 关方向。2022 年,这一领域又向前迈进了一大步,科研人员相继实现了利用重塑着丝粒周围异染色质 和重建非典型宽 H3K4me3 结构域的方法,将干细胞稳定培养成为全能样干细胞 (totipotent-like stem cells, TLSCs) ;将人类体细胞诱导重编程为全能 型8细胞期胚胎样细胞(eight-cell-like cells, 8CLCs); 以及利用小分子诱导因子组合,将小鼠 PSCs 诱导 成为类似于 2 细胞期胚胎的全能干细胞 (chemically induced totipotent stem cells, ciTotiSCs)等。 另 一 方面,化学重编程技术是由北京大学邓宏魁教授首 创的一种新型重编程技术,近年来该技术也不断发展成熟。2022 年,该领域获得了一系列新进展,实现了将人类体细胞重编程至一种中间可塑性状态的 多能干细胞 (chemically induced pluripotent stem cells, CiPSCs) ;以及将人类成红细胞重编程为巨核细胞和血小板,为这两种细胞人工大规模制备奠定了基础 。
2.1.2 干细胞疾病治疗研究展现可观发展潜力 在干细胞疾病治疗研究方面,多种疾病的干细 胞疗法都得到进一步推进。糖尿病的干细胞疗法被 美国《时代》周刊评选为“未来十年医疗 12 大创 新发明”之一。2022 年,科研人员对干细胞向胰岛 细胞的分化方案进行了进一步优化,构建出了结构 和功能更加仿生的胰腺 β 细胞 ,并通过体外实 验、小鼠实验、非人灵长类动物实验对其细胞功能 进行了全面评估,证实了干细胞来源的胰岛细胞用 于糖尿病研究和治疗的可行性,为胰岛 β 细胞的体 外规模化制造奠定了基础,而在非人灵长类动物体 内的效果验证更是标志着糖尿病干细胞疗法朝着临 床转化迈出了实质性的一步。与此同时,科研人员 还针对相关细胞移植过程中的免疫排斥问题进行了深入探索,利用经过基因编辑的干细胞衍生胰腺细 胞,实现了在不使用免疫抑制剂的情况下对糖尿病 患者进行移植治疗 ,成为寻找胰岛素产生细胞 替代品 20 年研究进程中的重要突破。此外,干细胞疗法与基因疗法的融合还为一系列罕见病的治疗带来了全新的希望。科研人员进一步证实了干细胞 结合基因疗法治疗渐冻症的疗效和安全性 ,同 时也证实了自体造血干细胞结合基因疗法能够显 著缓解早发异染性脑白质营养不良 (metachromatic leukodystrophy, MLD) 的症状 。
2.1.3 干细胞产业发展有序推进
在产业发展方面,2022 年全球共启动了干细 胞相关临床试验超过 400 例,使全球干细胞临床试 验累积至 7 500 余例 ( 数据来源 :ClinicalTrials.gov 数据库 ),其中免疫系统疾病、移植物抗宿主病、白血病、淋巴系统疾病、肿瘤疾病以及血管疾病是 研究较多的疾病类型。此外,干细胞相关产品的上市进程也同样有序推进。2022 年,美国 FDA 批准 了 Bluebird 公司开发的自体造血干细胞基因疗法 Zynteglo (betibeglogene autotemcel)上市,用于治疗β地中海贫血。该药物此前曾获得欧盟的上市许可,并获得 FDA 的孤儿药和突破性疗法认定。同时,美国和日本的两家公司又分别向监管机构提交了一 种新型干细胞产品的上市申请。其中,Gamida 公 司研发的 Omidubicel 获得了 FDA 授予的优先评审资格,该产品是首个获得美国 FDA 突破性疗法认定的骨髓移植治疗产品,而且在美国和欧盟都获得 了孤儿药资格认证,用于治疗多种恶性血液疾病。SB623 是由日本 Sanbio 公司开发的一种经过基因修 饰的间充质干细胞产品,用于治疗外伤性脑损伤。 2022 年 3 月,该公司完成了向日本厚生劳动省 (MHLW) 的产品生产和上市申请。 自 2016 年我国规范了干细胞技术和产品的备案政策后,我国干细胞疗法的转化进程也逐渐加快,一系列干细胞研究成果实现了临床转化。截至 2022 年,备案的临床试验数量已超过 100 例,批准设立的干细胞临床研究备案机构也近 140 家。此外,自 2018年干细胞按药品和技术“双轨制”监管制度管 理以来,企业的研发积极性逐渐上升。2022 年,国 家药品监督管理局药品审评中心 (CDE) 共受理了干 细胞相关药物的临床试验申请 21 项,其中获得临床试验默示许可的药物有 15 项 ( 表 1)。 至 此,CDE 受理干细胞 / 祖细胞新药申请的数量累积至 43 项,共计 35 项获得临床默示许可。
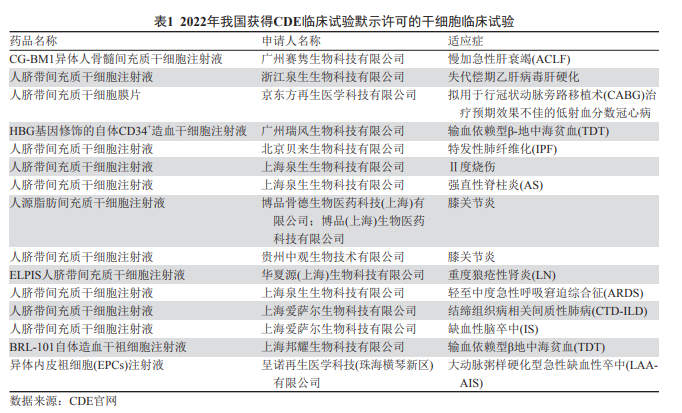
2.2 类器官领域进入技术爆发期
广义的类器官是人工构建的仿生组织器官的统 称,近年来处于发展最前沿的包括基于干细胞的类 器官技术和器官芯片技术两类。这两类技术一经出现,便引起了国际广泛关注,先后被评选为 Science 杂志 2013 年十大突破、2016 年世界经济论坛“十 大新兴技术”之一、Nature Methods 2017 年度技术。经过十余年的密集发展,在疾病研究、药物筛选、 药效测试、药物敏感性检测等方面展现出广阔且可 靠的应用前景,有望成为传统动物模型的补充甚至 替代。近年来,该领域发展逐渐加速,进入了技术爆发和科研成果井喷的阶段,而相关产业也初具雏形,孕育了巨大的产业价值。
2.2.1 类器官技术快速优化
2022 年,干细胞来源类器官在结构和功能中 的仿生性进一步提升,这也是该领域现阶段发展的重点。科研人员突破性地实现了人类大脑类器官与 大鼠大脑的连接,进而促进了人脑类器官的发育成 熟,实现了人类神经元与大鼠神经元的突触连接并 影响大鼠的行为 ;还利用小鼠胚胎干细胞在体外 构建出合成胚胎 (synthetic Embryo, sEmbryo) 模型, 其中发育出大脑和跳动的心脏。这些模型为研究 哺乳动物发育和早期器官发生过程提供了全新的工具平台。此外,科研人员还不断优化类器官的构建 策略,构建出含有胃窦和胃底组织以及腺体和神经的胃类器官、含有成熟潘氏细胞的小肠类器官、泪腺类器官等。在器官芯片领域,多器官芯片 乃至人体芯片的构建是该领域发展的最终目标, 2022 年这一进程得到推进,科研人员利用人工心脏、 骨骼、肝脏和皮肤开发出一种“即插即用”的多器官芯片,高度还原了人体内的生理结构和器官之间的连通。此外,基于干细胞的类器官和器官芯片技术逐步融合,发展出类器官芯片这一全新的技术 方向,为类器官领域的发展带来了新机遇。2022 年, 科研人员构建出肝脏 - 胰岛类器官芯片,在体外模拟人体肝脏 - 胰岛轴及其在生理和病理条件下的糖刺激响应,为糖尿病等代谢性疾病研究和相关药物开发提供了新平台 。
2.2.2 类器官展现广阔应用前景,产业发展开始起步
在类器官技术不断优化的基础上,多种类器官作为一种全新的生物模型在多个场景中展现广阔的 发展前景。在科研方面,类器官为多种生理、病理 机制的探索提供了全新的机遇,如利用大脑类器官 研究了自闭症风险基因的分子机制 ,再现了人类大脑发育过程中的关键事件 ,揭示了大脑的发 育机制 ,以及利用直肠癌类器官揭示了直肠癌化 疗后易复发的分子机制等。药物研发是类器官另一个主要的应用场景,类 器官在该领域的应用有助于缩短药物研发周期,降低开发成本与风险,并为药物的标准化筛选带来发 展新契机。这一应用领域目前已经进入了初步的产业化发展阶段。一方面,从早期开展类器官研发的 领先机构中,已经衍生出一批专注于类器官研发的 企业,如源自荷兰 Hubrecht 研究所的 HUB 公司、 源自美国康奈尔大学的 Hesperos 公司、源自美国哈 佛大学的Emulate 公司等。随着技术的不断成熟, 这些企业陆续开始与药企建立合作,针对药物研发 需求开发针对性的类器官模型。而另一方面,多家 全球知名的大型药物研发企业也陆续开始进军这一 领域,在新药研发中引入类器官技术。2022 年这一 进程继续推进,百时美施贵宝 (BMS) 和赛诺菲 (Sanofi) 分别与类器官研发公司 Prellis 建立合作, 利用其研发的淋巴结类器官平台开展抗体研发。 Crown Bioscience 则与 HUB 公司合作,首次基于类 器官对细胞药物进行筛选和表征,完成了临床前研 究。此外,干细胞研究公司 STEMCELL Technologies 还与 HUB 公司签署了扩大合作协议,共同开展基 于类器官的临床前毒理学筛选和非癌症药物开发服 务。在这一进程的推动下,类器官作为药物开发临 床前模型的应用在 2022 年首次获得了政府层面的 认可。Sanofi 利用 Hesperos 公司开发的体外微生理 系统,针对慢性炎性脱髓鞘性多发性神经病 (chronic inflammatory demyelinating polyradiculoneuropathy, CIDP) 和多灶性运动神经病 (multifocal motor neuropathy, MMN) 两种罕见的自身免疫性疾病开展了临床前研究 , 获得的研究数据获得了 FDA 认可,相关药物进入 临床试验 (NCT04658472)。这是 FDA 批准的全球 首个完全基于类器官芯片研究获得临床前数据的新 药进入临床试验。
2.3 异种器官移植迎来全新发展机遇
器官移植领域一直受制于器官捐赠不足的困 境,异种器官移植是科学家针对这一问题所开辟出 的一条获取移植器官的路径。利用与人类亲缘关系 较近且体型类似的动物,例如猪作为器官供体,存 在较少的伦理问题,而且数量充足,理论上非常有 希望成为稳定的器官来源。然而,由于存在技术瓶 颈和伦理问题,猪器官的异种移植在近 20 年的时 间内一度停滞不前。近年来,随着以基因编辑技术 为代表的基因改造技术的快速优化和革新,猪器官 的异种移植研究迎来了全新发展机遇,这一沉寂多 年的领域开始焕发新的生机。 2021 年是人类异种器官移植具有里程碑意义 的一年,科研人员利用 Revivicor 公司构建的“GalSafe 猪”实现了猪器官在脑死亡患者体内的移植,并证 实这一器官能够在人体中发挥作用。在这一基础上,2022 年 1 月,美国马里兰大学医学中心的科研人员 同样利用“GalSafe 猪”作为器官供体,为心力衰竭患者进行了猪心脏的异体移植,该手术获得了美 国 FDA 的紧急授权,即当患者的生命安全受到威 胁又没有其他选择时可以使用。手术几周后,患者 体内的移植心脏发挥了正常功能,且没有出现排异 反应,最终接受移植的患者存活了 2 个月。这一手 术为异种器官移植提供了宝贵的经验,也为患有心 脏、肾脏及其他器官疾病的患者带来了新希望。
3 再生医学领域未来展望与趋势
首先,在干细胞领域,随着学科交叉融合的日 趋深入以及生物技术的不断进步,对干细胞相关机 制将获得越来越全面和深刻的认识,从而为干细胞疗法的研发提供更加充足的证据。在此基础上,干细胞领域的发展路径也不断拓展,尤其是干细胞疗法与免疫疗法、基因疗法等新型疗法的联用将发挥 协同效应,为疾病治疗提供更多的潜在解决方案。 随着各国对干细胞疗法临床转化和产业化发展更加 重视,干细胞疗法的转化进程将逐渐加快,产业化体系发展规模也将日趋扩大,但同时也要看到,目前已经上市的干细胞药物或治疗技术都尚未形成规 模化应用,因此,未来开展干细胞药物规模化生产技术和体系研究,以及开展卫生经济学研究,对于充分发挥干细胞疗法对健康的促进作用至关重要。 其次,在类器官领域,随着相关技术的进一步 成熟,类器官作为一种新型的生物模型具有巨大的 发展潜力,既能够避免动物模型与人体的差异问题, 在体外接近真实地重现人体器官的生理、病理活动; 还能够利用患者的细胞构建出具有疾病特征的组织 器官模型,极大地扩充了疾病模型的种类。此外,类器官模型的构建周期短,能够满足各类应用场景 对生物模型的差异化、规模化需求,成为制药业和 精准医学发展的重要支撑。未来,在国际上对动物实验替代、减少和优化 (3R) 的呼声越来越高涨的 背景下,随着类器官技术的不断优化,类器官将有 望成为动物模型的补充甚至替代,进而变革药物研 发、药物评估和疾病研究等领域的发展模式。 最后,在异种器官移植领域,2021 年和 2022 年的一系列探索为这一沉寂多年的领域带来了发展 的新希望。未来,基因编辑等基因工程技术的进一 步革新、对异种器官和人类差异认识的不断深入、新型免疫抑制剂的开发以及科学高效的围手术期管 理策略的建立 ,将有望进一步延长异种器官的存活率,促进异种器官移植在人类疾病治疗中的应用。
版权声明:
本网站所有注明"来源:华大集团"或“来源:华大医疗”的文字,图片和音视频资料,版权均属于华大集团所有。非经授权,任何媒体,网站或个人不得转载,授权转载时须注明“来源:华大集团”。本站仅负责审核内容合规,其内容不代表本站立场,本站不负责内容的准确性和版权。如果存在侵权,或不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。




